Angew:两种同构吡啶-羧酸铜骨架中二氧化碳和乙炔的反向分离
发布日期:2024-06-11 来源:BB电子官网平台网址 热门游戏尽在掌握v7.2.11仪器

背景介绍
全文速览
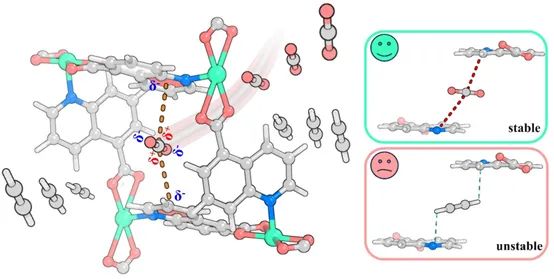
图文解析
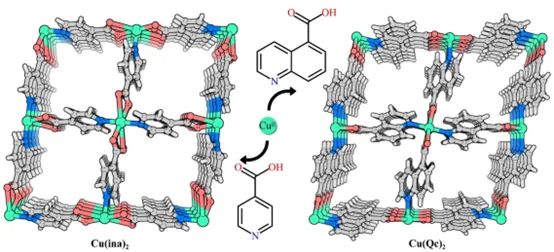
要点:Cu(Qc)2和Cu(ina)2的结构都是由通过π-π堆叠相互作用堆叠的二维配位网络组成的,其中每个Cu(II)原子都由两个羧基和两个吡啶基/喹啉基配位。在它们的层状结构中,Cu原子作为4个连接的节点,由2个连接的配体连接,形成方格(sql)网。去除溶剂分子后,Cu(Qc)2和Cu(ina)2都显示出一维孔道,可利用的空隙空间分别为17.2%和22.3%。它们的孔腔尺寸分别约为4.7×6.1×6.6和5.4×5.8×6.3 Å3,可容纳CO2和C2H2。它们在孔腔相互连接处的孔径仅约为3.3 Å和4.1 Å,与CO2和C2H2分子的最小横截面积大小相吻合。
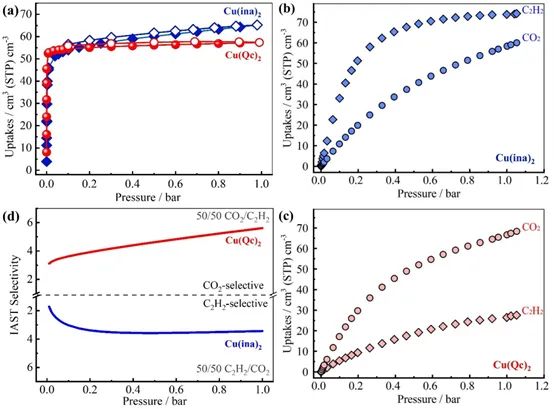
要点:如上图a所示,在195 K时,两种MOF对CO2的吸附能力相似,测量结果显示它们具有相似的BET数值。常温下单组份吸附等温线结果显示,Cu(ina)2对C2H2具有选择性吸附作用,而在相同的条件下,Cu(Qc)2对CO2具有较高的选择性吸附。Cu(Qc)2对CO2的吸附能力高于Cu(ina)2,这可能是由于Cu(Qc)2中更强的主客体相互作用。根据CO2和C2H2的单组分吸附等温线,利用理想吸附溶液选择性(IAST)理论评估了两种MOF的吸附选择性,在1 bar和298 K条件下,具有CO2选择性的Cu(Qc)2对等摩尔CO2/C2H2混合物的分离选择性为5.6,Cu(ina)2分离等摩尔C2H2/CO2混合物时的选择性为3.4。
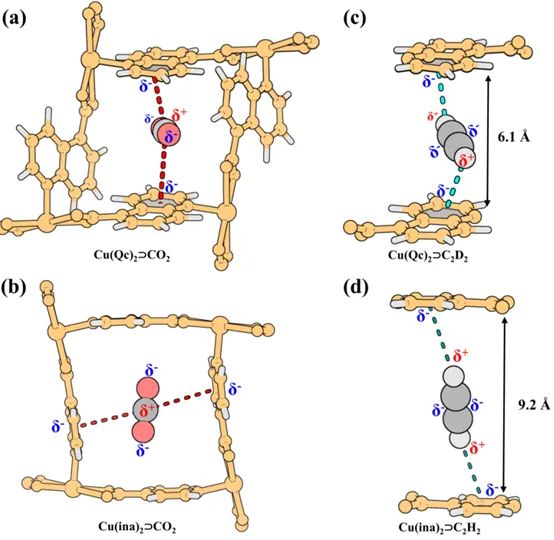
要点:为了进一步研究CO2和C2H2在Cu(Qc)2中的吸附位置,研究者进行了高分辨率中子粉末衍射(NPD)测量,成功确定了Cu(Qc)2中CO2和C2D2分子的结合构型。结果显示,二氧化碳分子位于侧向,其长轴与孔道方向相对平行(上图a, b)。二氧化碳分子通过πδ----Cδ+相互作用与相邻的芳香环相互作用,其中大部分相互作用比两个碳原子的范德华半径之和略短,表明存在相当大的静电作用。这些微弱的静电作用与容易再生的相对较低的吸附热是一致的。相比之下,C2D2分子与芳香环的结合构型不如其理想结合模型那么稳定。垂直于芳香环平面的理想正面结合构型被认为是炔烃分子的稳定构型,可使其与芳香环的静电相互作用达到最大化。然而,Cu(Qc)2中C2D2分子的结合方向与理想的正面结合构型有很大偏差,这是由于两个喹啉环之间的距离为6.1-7.2Å,比理想的正面结合构型的8.9Å要短。因此,这两个分子在Cu(Qc)2紧凑的孔隙空间中相反的结合构型导致了CO2对C2H2的反向选择性吸附。
GCMC模拟计算得出的CO2和C2H2结合构型与NPD数据的实验结果一致。总的来说,紧凑的孔径和相对不太稳定的结合构型阻碍了普通MOF中通常很强的可极化C2H2的吸附,从而逆转了选择性吸附。相比之下,孔径较大的Cu(ina)2中结合的C2H2分子更接近理想构型(上图c, d),这使得Cu(ina)2能够优先吸附C2H2而不是CO2。
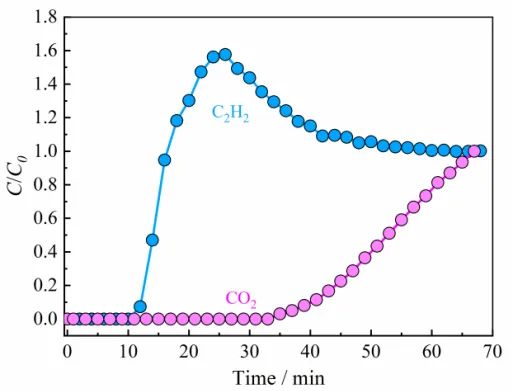
要点:穿透实验结果证实了Cu(Qc)2的实际CO2/C2H2分离性能,实际分离结果表明,Cu(Qc)2可以在单步分离过程中产生纯净的C2H2,预计高纯度C2H2的生产率为160 mmol kg-1,与CO2选择性MOF Cu-F-pymo的生产率相当。
总结与展望
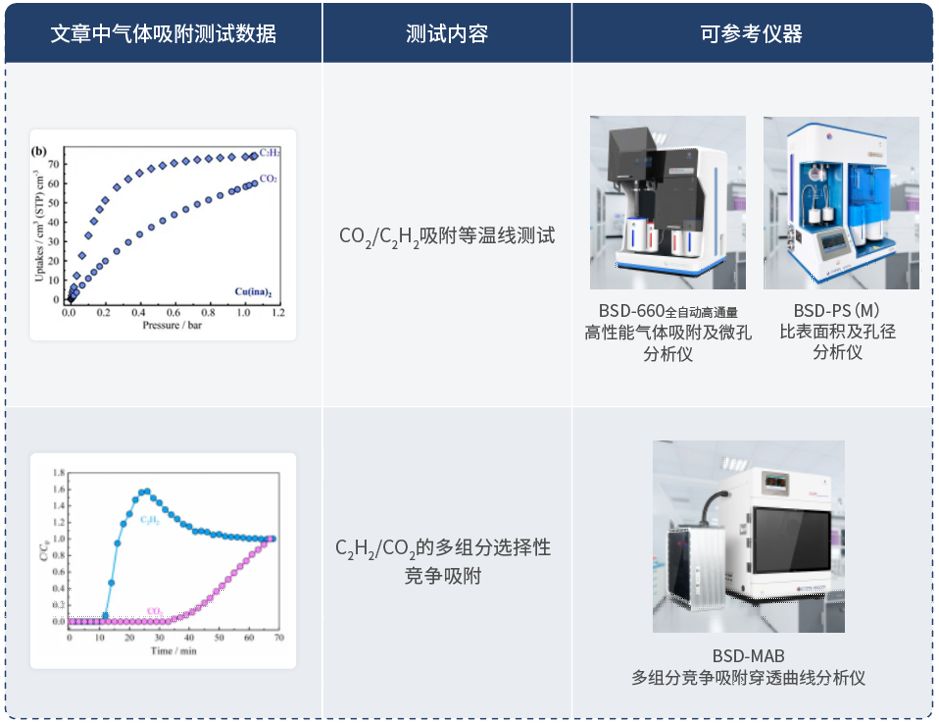
BB电子官网平台网址 热门游戏尽在掌握v7.2.11 吸附表征 全系列测试方案

测样、送检咨询:杨老师
138 1051 2843(同微信)








